1.
Поставьте в соответствие характеристики и определения.
|
Единица количества вещества |
|
|
6,02⋅1023 моль-1 |
|
|
1,66057⋅10-24 г |
|
|
Молярная масса вещества |
|
|
Массовая доля вещества |
|
|
Величина 22,4 л/моль |
|
|
Мольная доля вещества |
|
|
Молярная концентрация |
|
2.
Какова масса метана (в г), содержащего 1,204 · 1024 молекул?
3.
Определите массовую (ω) и мольную (φ) доли водорода в этаноле.
4.
Какую массу (в г) имеет смесь пропана и бутана объемом 100 л при нормальных условиях, если объемная доля каждого газа равна 50%?
5.
Масса 200 мл (при н.у.) ацетилена равна 0,232 г. Определите молярную массу ацетилена.
(Не забудьте указать размерность найденной величины!)
6.
При сжигании смеси этана и циклопропана массой 8,8 г образовался оксид углерода(IV) объемом 13,44 л (н.у.). Определите массовую долю циклопропана в данной смеси (в %).
7.
При сжигании 50 г пропана получили оксид углерода(IV) объемом 67,2 л (н.у.). Вычислите, весь ли пропан был израсходован.
8.
При нагревании этанола массой 4,6 г с уксусной кислотой массой 7 г получили сложный эфир. Какова масса этого продукта в граммах?
Ответ округлите до целого числа.
9.
На сжигание 105,26 м3 природного газа потребовалось 1000 м3 воздуха. Вычислите объёмную долю метана в природном газе (в %), считая, что остальные примеси в нем не горючи. Объёмная доля кислорода в воздухе равна 20%.
10.
Сколько граммов бромной воды с массовой долей брома 1,6% может обесцветить пропилен объёмом 1,12 л (н.у.)?
11.
Вычислите массу (в г) сахарозы, подвергшуюся гидролизу, с учетом того, что из образовавшейся глюкозы получена молочная кислота массой 54 г при массовой доле выхода 60%.
12.
На полное гидрирование этиленового углеводорода массой 14 г затрачен водород объемом 4,48 л (н.у.). Какова молекулярная формула этого углеводорода?
13.
Сколько миллилитров 96%-ного этанола (ρ=0,8 г/мл) потребуется для этерификации 1,5 г аминоуксусной кислоты, если спирт был взят с 200%-ным избытком? Ответ округлите до целого числа.
14.
Рассчитайте массу (в граммах) 1,1-дихлорэтана, который может быть получен из 280 л ацетилена при н.у., если массовая доля выхода этого вещества составляет 80%.
15.
Определите количество теплоты (в кДж), выделившейся при сгорании 0,25 моль этанола, используя уравнение реакции горения этого вещества:
C2H5OH + 3O2 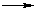 2CO2 + 3H2O + 1418 кДж
2CO2 + 3H2O + 1418 кДж