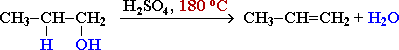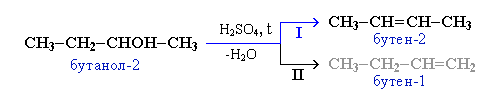Реакции дегидратации спиртов
Отщепление воды от молекул спирта (дегидратация спиртов) происходит при действии концентрированной серной кислоты и в зависимости от температуры может идти как внутримолекулярная или межмолекулярная реакция.
- Внутримолекулярная дегидратация спиртов осуществляется при повышенной температуре и приводит к образованию алкенов (реакция элиминирования):
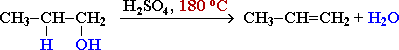 В тех случаях, когда возможны два направления реакции, например:
В тех случаях, когда возможны два направления реакции, например:
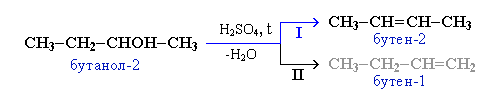
дегидратация идет преимущественно в направлении I, то есть по правилу Зайцева
– с образованием более замещённого алкена (водород отщепляется от менее гидрогенизированного атома углерода).
Легкость внутримолекулярной дегидратации спиртов уменьшается в ряду:
третичные > вторичные > первичные.
- Межмолекулярная дегидратация спиртов с образованием простых эфиров происходит при более низкой температуре, чем внутримолекулярная реакция:
 Отщепление молекулы воды от двух молекул спирта с образованием простого эфира можно рассматривать как реакцию нуклеофильного замещения группы HО– в одной молекуле спирта на группу C2H5O– (в общем случае RO–) от другой молекулы. При этом в одной молекуле спирта разрывается связь О–Н, а в другой – связь С–О. Данная реакция более характерна для первичных спиртов. Вторичные и третичные спирты в таких условиях обычно не образуют простых эфиров, а превращаются в алкены (то есть происходит реакция элиминирования).
Отщепление молекулы воды от двух молекул спирта с образованием простого эфира можно рассматривать как реакцию нуклеофильного замещения группы HО– в одной молекуле спирта на группу C2H5O– (в общем случае RO–) от другой молекулы. При этом в одной молекуле спирта разрывается связь О–Н, а в другой – связь С–О. Данная реакция более характерна для первичных спиртов. Вторичные и третичные спирты в таких условиях обычно не образуют простых эфиров, а превращаются в алкены (то есть происходит реакция элиминирования).
Таким образом, активность спиртов при межмолекулярной дегидратации:
СН3ОН > первичные > вторичные > третичные.
Реакции элиминирования и нуклеофильного замещения могут протекать одновременно и конкурировать между собой. Изменение условий (в данном случае, температуры) позволяет осуществить преимущественно одну из этих реакций. Важным фактором является и строение спирта. Для третичных спиртов легче идет внутримолекулярная дегидратация (элиминирование), а для первичных – межмолекулярная (замещение).